今日(6月12日),中国国家药监局药品审评中心(CDE)官网公示,乐普生物1类新药MRG007获批临床,拟开发治疗局部晚期或转移性实体瘤。公开资料显示,这是一款靶向CDH17的抗体偶联药物(ADC)。今年1月,ArriVent BioPharma和乐普生物宣布达成全球独家许可协议,获得该产品在大中华区以外地区开发、制造和商业化的全球独家许可。乐普生物将获得总计4700万美元的一次性首付款和近期里程碑付款,和最高达11.6亿美元的开发、注册和销售等里程碑付款。
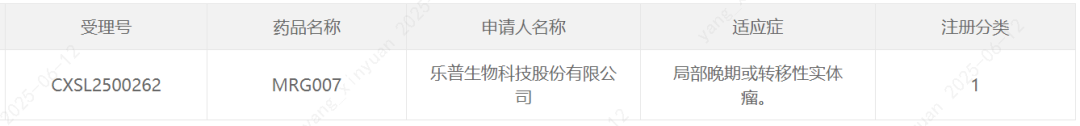
CDE官网
钙黏蛋白17(CDH17)是一种膜细胞黏附分子,其在CRC及其他多种胃肠道(GI)癌症中频繁过表达,而在正常肠组织与胰腺导管中表达有限。这种肿瘤与正常组织间的差异表达特征,使其成为胃肠道癌症(尤其是CRC)抗体偶联药物(ADC)开发的理想靶点。
MRG007是一种靶向CDH17的ADC,由新型人源化IgG1抗体通过定点偶联细胞毒素Exatecan而成,具有平衡的药物抗体比(DAR)。这一差异化设计有望提升抗肿瘤疗效并拓宽治疗窗。

在今年3月的美国癌症研究协会(AACR)年会上,研究人员公布了MRG007的临床前研究结果。研究表明,在多种CDH17表达水平的胃肠道肿瘤模型和结直肠癌模型中,MRG007表现出显著且剂量依赖的肿瘤生长抑制作用。探索性毒理研究中MRG007展现出良好的PK特性与安全耐受性。研究人员认为,MRG007作为一种差异化且高效的ADC候选药物,具备进入CDH17表达癌症临床试验的潜力。
本次这款ADC新药在中国获批临床,意味着其即将进入临床研究阶段。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.From https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2]2877 / 16 - MRG007, a cadherin 17-targeted, glycan-linked, exatecan-based antibody-drug conjugate, demonstrated potent anti-tumor activity and a good safety profile in preclinical studies. Retrieved Apr 28, 2025. From https://www.abstractsonline.com/pp8/#!/20273/presentation/3103
